РАЗДЕЛ II. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Основные законы и формулы
Примеры решения задач
Задачи для самостоятельного решения
Качественные задачи
Контрольные вопросы
Решая задачи на применение уравнения Клапейрона - Менделеева, не следует забывать, что данное уравнение описывает состояние идеального газа. Кроме этого надо помнить, что все применяемые в этом разделе физические величины имеют статистический характер. Полезно, приступая к решению задач, нарисовать эскизно график процесса, с подходящими переменными по координатным осям.
Основные законы и формулы
| Количество вещества | 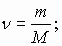 или или  |
Уравнение Клапейрона-Менделеева
(уравнение состояния идеального газа) | 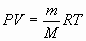 |
| Закон Дальтона |  |
| Концентрация молекул | 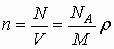 |
| Уравнение молекулярно-кинетической теории газов | 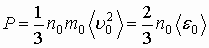 |
| Средняя кинетическая энергия одной молекулы идеального газа (внутренняя энергия) | 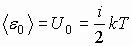 |
| Внутренняя энергия массы идеального газа |  |
| Уравнение Майера |  |
| Теплоёмкость молярная и её связь с удельной |  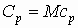
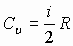  |
| Первое начало термодинамики | 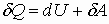
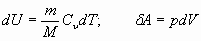 |
| Работа расширения газов в процессах: | |
| адиабатном | 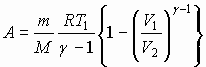 |
| изотермическом |  |
| изобарном | 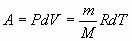 |
| Уравнение Пуассона, связывающее параметры газа в адиабатном процессе |  ; ; 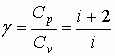 |
| Изменение энтропии | 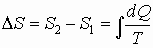 |
| Термический к.п.д. цикла Карно | 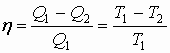 |
Примеры решения задач
Пример 4. Кислород массой 320г. Нагревают при постоянном давлении от 300K до 310К. Определить количество теплоты, поглощенное газом, изменение внутренней энергии и работу расширения газа.
Дано: m=320г=0,32кг; T1=300 K; T2=310 K
Найти: Q, ΔU, A
Решение: Количество теплоты, необходимое для нагревания газа при постоянном давлении определим, используя I начало термодинамики:
Здесь Cp - молярная изобарная теплоёмкость, М - молярная масса газа;
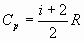 , где i = 5 для кислорода, как двухатомного газа; , где i = 5 для кислорода, как двухатомного газа;
М =32кг/кмоль.
Подставляя в (1) числовые значения, получим:

Изменение внутренней энергии газа:
подставляя числовые значения и учтя, что 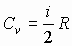 , получим , получим
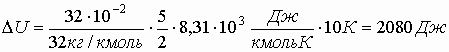
Работа расширения газа при изобарном процессе:
где Δ
V=V2-V1 - изменение объёма газа при расширении можно найти из уравнения Клапейрона-Менделеева:
Для двух состояний газа при изобарном процессе:
и тогда вычитая почленно (5) из (4), получим:
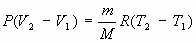 и подставляя в (3), находим: и подставляя в (3), находим:
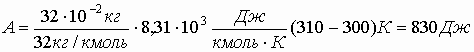
Проверка: Q= Δ
U+A; 2910Дж = (2080 +830) Дж
Ответ: Q = 2910Дж; Δ
U = 2080Дж; A = 830Дж
Пример 5. Найти среднюю кинетическую энергию вращательного движения одной молекулы кислорода при температуре T = 350K, а также кинетическую энергию вращательного движения всех молекул кислорода массой 4г.
Дано: T = 350K; m = 4г = 4·
10-3кг; M = 32кг/кмоль
Найти: áε
врñ0; Eквр
Решение: На каждую степень свободы молекулы газа приходится одинаковая средняя энергия 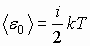 , где k - постоянная Больцмана; T - абсолютная температура газа. Так как вращательному движению двухатомной молекулы O2 соответствует две степени свободы, то средняя энергия вращательного движения молекулы кислорода будет , где k - постоянная Больцмана; T - абсолютная температура газа. Так как вращательному движению двухатомной молекулы O2 соответствует две степени свободы, то средняя энергия вращательного движения молекулы кислорода будет
Подставив в (1) значения k = 1,38·
10-23Дж/K и T = 350K , получим
áε
врñ0 = 1,38·
10-23Дж/K·
350K = 4,83·
10-21Дж.
Кинетическая энергия вращательного движения всех молекул газа определяется Eквр=N·
áε
врñ0 (2)
Число всех молекул N газа вычислим по формуле
где NA -число Авогадро; ν
= m/M - количество вещества.
Подставив это в (3), получим N = NA·
m/M.
Теперь подставим это в (2):
Eквр = N·
áε
врñ0 = NA·
(m/M)·
áε
врñ0.
Подставим численные значения, получим:
Eквр = 6,02·
10-23моль-1·
4,83·
10-21Дж ·
4·
10-3кг/(32·
10 -3кг/моль) = 364Дж.
Ответ: áε
врñ0 = 4,83·
10-21Дж; Eквр=364Дж
Пример 6. Как изменится энтропия 2г водорода, занимающего объем 40л при температуре 270К, если давление увеличить вдвое при постоянной температуре, а затем повысить температуру до 320К при постоянном объёме.
Дано: m=2г =2·
10-3кг; М=2кг/кмоль; V=40л=4·
10-2м3.
T1=270K; T2=320K ; P2=2P1
Найти: Δ
S
Решение: Изменение энтропии определяется формулой:
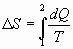 , ,
где dQ- количество теплоты, полученное в данном процессе.
Изменение энтропии согласно условию происходит за счет двух процессов:
1) изотермического и 2) изохорного. Тогда:
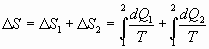
Количество теплоты dQ1 и dQ2 найдем из 1 начала термодинамики для этих процессов:
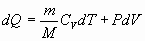
1) dQ1=PdV (т.к. dT=0 для T=const)
P найдем из уравнения Клапейрона-Менделеева:
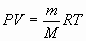 , тогда , тогда  и и
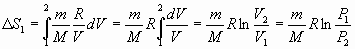 ; ;
т.к. при T=const, P1V1=P2V2
2) 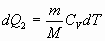 (т.к. dV=0 и dA=0 при V=const) (т.к. dV=0 и dA=0 при V=const)
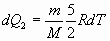 и и 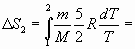
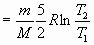 ; ; 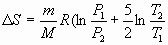
Подставляя численные значения, получим:
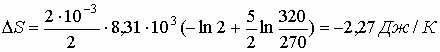
Ответ: Δ
S = -2,27 Дж/K
Задачи для самостоятельного решения
51. В баллоне ёмкостью 10л находится сжатый воздух при температуре 27°C. После того как часть воздуха выпустили, давление понизилось на 2·105 Па. Определить массу выпущенного воздуха. Процесс считать изотермическим.
52. Какой объём занимает при нормальных условиях смесь 4кг гелия и 4кг азота?
53. В сосуде, имеющем форму шара, радиус которого 0,2м, находиться 80г азота. До какой температуры можно нагреть сосуд, если его стенки выдерживают давление 7·105 Па.
54. При температуре 27°C и давлении 12·105 Па плотность смеси водорода и азота 10 г/дм3. Определить молярную массу смеси.
55. В баллоне ёмкостью 5л находиться 2кг водорода и 1кг кислорода. Определить давление смеси, если температура окружающей среды 7°C.
56. Давление идеального газа 2МПа, концентрация молекул 2·103 см-3. Определить среднюю кинетическую энергию поступательного движения одной молекулы и температуру газа.
57. Определить среднюю кинетическую энергию вращательного движения одной молекулы двухатомного газа, если суммарная кинетическая энергия молекул в 1кмоле этого газа 6,02Дж.
58. Найти среднюю кинетическую энергию вращательного движения всех молекул, содержащихся в 0,25г водорода при температуре 27°C.
59. Определить концентрацию молекул идеального газа при температуре 350К и давлении 1,0МПа.
60. Определить температуру идеального газа, если средняя кинетическая энергия поступательного движения его молекул 2,8·10-19 Дж.
61. Найти увеличение внутренней энергии и работу расширения 30г водорода при постоянном давлении, если его объём увеличился в пять раз. Начальная температура 270К.
62. Азот массой 1кг, находящийся при температуре 300К сжимают: а) изотермически; б) адиабатно, увеличивая давление в десять раз. Определить работу, затраченную на сжатие в обоих случаях. Какое количество теплоты нужно сообщить 1моль кислорода, чтобы он совершил работу 10Дж: а) при изотермическом процессе; б) при изобарном?
63. Определить, какое количество теплоты необходимо сообщить углекислому газу массой 440г, чтобы нагреть его на 10К: а) изохорно, б) изобарно.
64. При нагревании 0,5кмоль азота было передано 1000Дж теплоты. Определить работу расширения при постоянном давлении.
65. Газ, занимающий объем 10л под давлением 0,5МПа, был изобарно нагрет от 323K до 473К. Найти работу расширения газа.
66. Газ, занимающий объем 12л под давлением 0,2МПа. Определить работу, совершенную газом, если он изобарно нагревается от 300K до 348К.
67. Найти работу и изменение внутренней энергии при адиабатном расширении 0,5кг воздуха, если его объем увеличится в пять раз. Начальная температура 17°С.
68. Определить количество теплоты, сообщенное 14г азота, если он был изобарически нагрет от 37°С до 187°С.. Какую работу он совершит и как изменится его внутренняя энергия?
69. Во сколько раз увеличится объем 2моль водорода при изотермическом расширении при температуре 27°С, если при этом была затрачена теплота 8кДж.
70. Определить молярную массу газа, если при изохорном нагревании на 10°С 20г газа потребуется 680Дж теплоты, а при изобарном 1050Дж.
71. Чему равно изменение энтропии 10г воздуха при изохорном нагревании от 250K до 800К?
72. При изобарном расширении водорода массой 20г его объем увеличился в три раза. Определить изменение энтропии водорода при этом процессе.
73. При изохорном нагревании 480г кислорода давление увеличилось в 5 раз. Найти изменение энтропии в этом процессе.
74. Объем гелия, массой 1кг , увеличился в 4 раза: а) изотермически б) адиабатно. Каково изменение энтропии в этих процессах?
75. Найти изменение энтропии при нагревании 1кг воды от 0°С до 100°С и последующем превращении ее в пар, при той же температуре.
76. Как изменится энтропия при изотермическом расширении 0,1кг кислорода, если при этом объем изменится от 5л до 10л?
77. Определить изменения энтропии при изобарном нагревании 0,1кг азота от 17 °С до 97°С .
78. Лед, находящийся при температуре -30°С, превращается в пар. Определить изменения энтропии в этом процессе.
79. Чему равно изменение энтропии 10г воздуха при изобарном расширении от 3л до 8л.
- Чему равно изменение энтропии 20г воздуха при изобарном охлаждении от 300K до 250К?
Качественные задачи
81. Объем газа уменьшили в 3 раза, а температуру увеличили в 2 раза. Во сколько раз увеличилось давление газа? Газ считать идеальным.
82. Сжатую пружину растворили в кислоте. На что пошла потенциальная энергия упругой деформации пружины?
83. Предлагаем два варианта объяснения подъемной силы воздушного шара, наполненного водородом. Согласно первому - подъемная сила - сила Архимеда. Согласно второму - подъемная сила возникает из-за разности в давлении на верхнюю и нижнюю части шара. Чем различаются эти объяснения?
84. Объясните, почему изотермическое расширение газа возможно только при подведении к нему количества теплоты?
85. Существует ли процесс, при котором все переданное рабочему телу от нагревателя тепло превращается в полезную работу?
86. Можно ли всю внутреннюю энергию газа превратить в механическую работу?
87. Почему КПД двигателя внутреннего сгорания резко падает при взрывном сгорании горючей смеси?
88. Как изменится температура в помещении, если дверцу работающего холодильника оставить открытой?
89. При нагревании двухатомного газа его теплоемкость в области высоких температур имеет резкий рост с последующим спадом. Аналогичная зависимость наблюдается и у многоатомных газов. Чем это объяснить?
90. Некоторый газ переходит из состояния I в II сначала по изохоре, а затем по изобаре. В другом случае сначала по изобаре, затем по изохоре. Будет ли в обоих случаях совершена одинаковая работа?
91. Почему нагревается насос при накачивании шины колеса автомобиля?
92. Почему металл и дерево одной и той же температуры на ощупь кажутся неодинаково нагретыми?
93. Можно ли вскипятить воду в бумажном стаканчике?
94. Почему капли воды на раскаленной плите "живут" дольше, чем на просто горячей?
95. Почему перед закипанием вода в чайнике "шумит"?
96. Почему вода в сосуде с крышкой закипает быстрее, чем без крышки?
97. Может ли воздушный шар в атмосфере Земли подняться на неограниченную высоту?
98. Кусок льда плавает в наполненном до краев сосуде с водой. Перельется ли вода через край, если лед растает?
99. Почему деревянный карандаш плавает в воде горизонтально? Объясните, почему он будет плавать вертикально, если к одному из его концов прикрепить груз?
100. Одинаковые свинцовые шарики опускают в равные по объему сосуды с водой. В одном сосуде температура воды 5°С, а в другом - 50°С. В каком сосуде шарик быстрее достигнет дна?
Контрольные вопросы
21. Что такое атом, молекула, ион?
22. Что называют термодинамической системой?
23. Что такое параметры состояния?
24. Какое состояние термодинамической системы называют равновесным, неравновесным?
25. Что такое идеальный газ?
26. Что характеризует уравнение состояния?
27. Дайте определение закона распределения Максвелла.
28. В чем заключается закон распределения Больцмана?
29. Что характеризует наиболее вероятная скорость?
30. Чему равна средняя арифметическая скорость?
31. Что такое теплота?
32. Дайте определение первого начала термодинамики.
33. Какие вы знаете изопроцессы?
34. Что представляет собой изотермический процесс?
35. Как вычислить работу газа изохорического и изобарического процессов?
36. Дайте определение адиабатического процесса.
37. Какие физические параметры связывает уравнение Майера?
38. Что такое теплоемкость тела, удельная и молярная теплоемкости?
39. О чем говорит второе начало термодинамики?
40. Как повысить КПД тепловой машины?
|